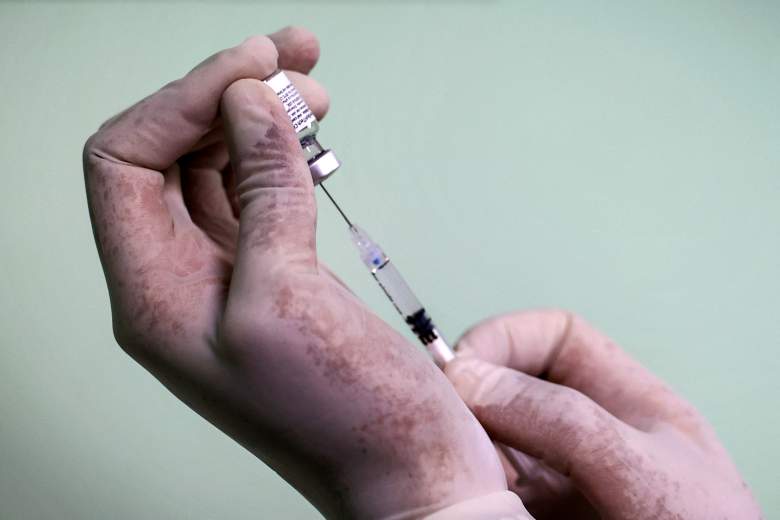
Getty Images
Este lunes la Administración de Drogas y Alimentos de (FDA, por sus siglas en inglés) de Estados Unidos ha otorgado la ‘aprobación total’ a la vacuna Pfizer/BioNTech contra el COVID-19, y se convierte así en la primera medicina de su tipo en ser habilitada por su comercialización para personas mayores de 16 años.
De acuerdo al comunicado emitido por la farmacéutica Pfizer, “la vacuna se conoce como la vacuna Pfizer-BioNTech COVID-19 y ahora se comercializará como Comirnaty (koe-mir’-na-tee), para la prevención de la enfermedad COVID-19 en personas de 16 años o más”.
Asimismo, Pfizer destaca que “la vacuna también sigue estando disponible bajo autorización de uso de emergencia (EUA), incluso para personas de 12 a 15 años de edad y para la administración de una tercera dosis en determinadas personas inmunodeprimidas”.
“La aprobación de esta vacuna por parte de la FDA es un hito a medida que continuamos luchando contra la pandemia de COVID-19. Si bien esta y otras vacunas han cumplido con los rigurosos estándares científicos de la FDA para la autorización de uso de emergencia, como la primera vacuna COVID-19 aprobada por la FDA, el público puede estar muy seguro de que esta vacuna cumple con los altos estándares de seguridad, eficacia y calidad de fabricación que requiere un producto para ser aprobado por la FDA”, dijo la comisionada interina de la FDA, Dra. Janet Woodcock, en declaraciones citadas en el comunicado de prensa.
En este sentido, la Dra. Woodcock subrayó la importancia que puede significar la aprobación de la FDA a la vacuna Pfier/BioNTech para que más personas confíen en su eficacia contra el Coronavirus y lleven a cabo la aplicación de la misma.
“Si bien millones de personas ya han recibido vacunas COVID-19 de manera segura, reconocemos que para algunos, la aprobación de una vacuna por parte de la FDA ahora puede infundir confianza adicional para obtener vacunado. El hito de hoy nos acerca un paso más a alterar el curso de esta pandemia en los EE. UU.”, aseguró la experta.
Qué diferencia existe entre la aprobación “para su uso de emergencia” y la aprobación “total” de la FDA
Si bien la vacuna Pfizer/BioNTech ya había sido aprobada para su uso de emergencia el 11 de diciembre de 2020, aún restaba la validación definitiva de la FDA. Pero, ¿Cuál es la diferencia entre ambos conceptos?
Según detalla la FDA, una medicina aprobada “para su uso de emergencia” puede ser implementada durante emergencias de salud pública para brindar acceso a productos médicos que pueden ser efectivos para prevenir, diagnosticar o tratar una enfermedad. Esto, siempre y cuando el citado organismo determine que los beneficios conocidos y potenciales de un producto, cuando se usa para prevenir, diagnosticar o tratar la enfermedad supere sus riesgos conocidos y potenciales.
En cambio, las vacunas aprobadas por la FDA se someten al proceso estándar de la agencia para revisar la calidad, seguridad y eficacia de los productos médicos. Para ello, la agencia evalúa los datos y la información incluidos en la presentación del fabricante de una Solicitud de Licencia de Biológicos (BLA, por sus siglas en inglés).
Un BLA es un documento completo que se envía a la agencia, en este caso la FDA, para proporcionar datos específicos del medicamento.
Y en gran parte, la “aprobación total” de la FDA a la vacuna de Pfizer/BioNTech contra el COVID-19 se debe al detallado BLA presentado por las autoridades de ambas compañías, como “datos e información preclínicos y clínicos, así como detalles del proceso de fabricación, resultados de las pruebas de vacunas para garantizar la calidad de las vacunas e inspecciones de los sitios. donde se fabrica la vacuna”, según indica el comunicado de los fabricantes.
Pfizer reporta que la seguridad de Comirnaty se evaluó en aproximadamente 22 mil personas que recibieron la vacuna y 22,000 personas que recibieron un placebo, todas de 16 años o más.
Según los resultados del ensayo clínico, la vacuna tuvo una efectividad del 91% en la prevención de la enfermedad COVID-19.
El Pentágono requerirá vacuna COVID-19 a sus miembros y empleados
A partir de la aprobación total que la FDA le otorgó a la vacuna Pfizer/BioNTech contra el Coronavirus, desde el Pentágono anunciaron que requerirán a sus empleados la vacuna para seguir trabajando en la sede del Departamento de Defensa de los Estados Unidos.
Según informa The Associated Press (AP), el portavoz del Pentágono, John Kirby, dijo que el secretario de Defensa Lloyd Austin está cumpliendo su promesa a principios de este mes de requerir las inyecciones una vez que la FDA haya aprobado la vacuna.
Además, Kirby adelantó que se está desarrollando una guía y se proporcionará un cronograma en los próximos días.
LEER MÁS: COVID-19: Duras penas por carnet de vacunación falso: ¿Cuánto años de cárcel?


